疫後醫療器材新商機:霧化器吸入給藥裝置
- 資料發布日期:112-09-07
- 最後更新日期:113-11-08
文/張益壽(工研院產服中心商業化整合部 )、林蕙鈴(長庚大學呼吸治療學系教授 )
疫情後,全球對呼吸系統健康議題的關切進一步攀升,加大了吸入式藥物傳遞裝置在醫療領域的需求。在這個領域,台灣廠商正面臨新的商機和挑戰。台灣在醫療器械的製造和生產技術方面具有卓越實力和豐富的經驗,能夠計算成本效益並提供高品質的產品。此外,台灣廠商都高度重視品質控制,確保產品符合國際標準和相關法規。
這些優越條件使台灣廠商能夠吸引來自國際市場的合作夥伴和客戶,特別是與歐美藥廠的合作機會,台灣廠商將有機會共同開發創新的吸入式藥物傳遞解決方案。然而,這些商機同時也帶來挑戰。隨著市場競爭的加劇,台灣廠商需要不斷提升技術和創新能力,以保持競爭力。此外,確保產品的合規性和安全性也是至關重要的,因為醫療器械領域的監督管理要求非常嚴格。
吸入給藥裝置主要類型
吸入給藥裝置是常見且有效的藥物傳遞方式,用於呼吸系統相關疾病的治療。以下是吸入給藥裝置的幾種主要類型(1):
- 定量吸入器(Pressurized Metered Dose Inhaler, pMDI):是一種使用壓力來釋放藥物的吸入裝置。它通常由金屬罐、噴霧閥和噴霧室組成,使用者透過噴霧閥按下,高壓釋放藥物形成微細懸浮液氣霧,然後通過嘴部或面罩進行吸入。pMDI需要使用者協調呼吸來確保藥物達到肺部。
- 乾粉吸入器(Dry Powder Inhaler, DPI):是一種將藥物以粉末形式提供給患者的吸入裝置。與pMDI不同,DPI不需要使用壓力或噴霧閥來釋放藥物。使用者通常需要通過吸氣的力量產生快速氣流,將吸入藥物帶到肺部。DPI的優點之一是不需要協調呼吸,但需要足夠吸氣力量產生快速氣流。
- 緩霧型氣霧吸入器(Soft Mist Inhaler, SMI):是一種提供藥物的吸入裝置。與pMDI類似利用壓力產生藥物釋放,不同之處在於SMI使用彈簧壓力將藥物轉換為緩慢釋放的懸浮液,形成微細的氣霧。這種氣霧可以以一致的速率釋放,讓使用者更容易吸入所需劑量。
- 霧化器(Nebulizer):是一種通過將藥水轉換為氣霧形式來傳遞的吸入裝置。霧化器使用壓縮空氣或超音波震動將藥物轉換為微細懸浮液,然後通過面罩、咬嘴或人工氣道遞送到患者肺部。霧化器適用於各個年齡段的患者,尤其適合年幼的兒童或無法協調使用其他吸入裝置的人群。
上述裝置中的前三種(pMDI、DPI和SMI)都屬於藥物專屬的吸入裝置,也是複合式產品,這意味著它們需要經過新藥查驗登記(New Drug Application, NDA)並獲得相應的上市許可,以確保裝置與特定藥物的結合是安全有效的。
霧化器則分為一般使用和藥物專屬兩種類型(2)。一般使用的霧化器需要通過510K類醫材認證取得上市許可,這種認證相對容易獲得,因此許多台灣和中國大陸的廠商生產這類產品,市場的競爭者也較多。相比之下,藥物專屬的霧化器需要配合藥品進行新藥查驗登記(NDA)取得上市許可,需要更多的臨床試驗和相關資料支持。因此,主要以歐美廠商為主。藥物專屬的霧化器都是跟吸入溶液一同銷售,也屬於複合式產品。
美國許可之II類醫材霧化器
根據美國FDA 510K資料庫(3),從2000年1月至2023年6底止,共有211筆II類醫材許可資料,其中涉及霧化器相關的許可有140筆,這些霧化器通常定義為一般使用霧化器。根據霧化器產生氣溶膠(Aerosol)的工作原理被分類為噴射霧化器(Jet nebulizer)獲得95筆許可,篩孔霧化器(Mesh nebulizer)獲得37筆許可,而超音波霧化器(Ultrasonic nebulizer)獲得8筆許可。
美國510K霧化器申請許可的流程,產品需要與已經在美國FDA合法上市的一種或多種相似產品(稱為「Predicate Device」)進行比對,證明其具有實質相等性,才能獲得許可。比對是為了確保新產品的安全性和有效性與已驗證的產品相當。值得一提的是,台灣的廠商在霧化器產品方面共獲得了25筆許可,皆是利用證明其產品與相似產品具有實質相等性之申請路徑取得許可,如表一所示。
由於美國510K霧化器認證較容易,導致市場上競爭者眾多,台灣廠商需要有獨特的產品價值和優勢、提高質量、更好的使用者體驗及品牌行銷策略,才有機會與其他競爭對手區隔,並擴大市佔,不然只能降低產品價格吸引客戶。
表一:取得美國510(K)二類霧化器醫材許可之台灣廠商
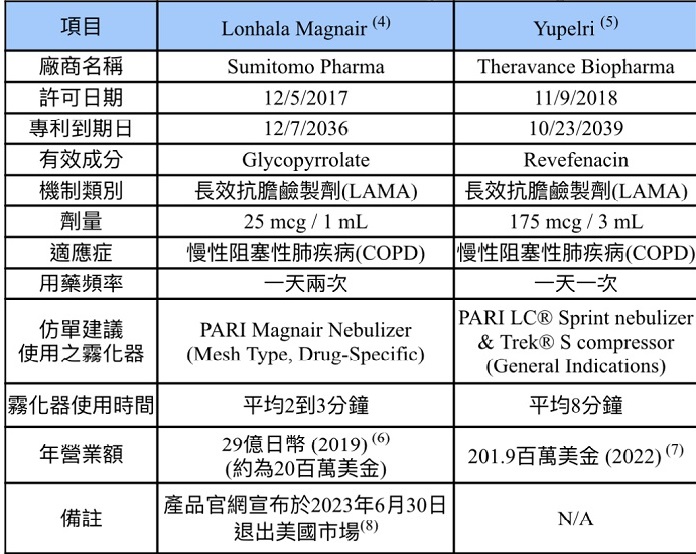
資料來源: 美國FDA 510K資料庫
霧化器複合式產品的比較優勢
霧化器複合式產品在市場上比較有優勢嗎? 以Lonhala Magnair跟Yupelri這兩個同為長效抗膽鹼製劑 (LAMA)用於治療慢性阻塞性肺疾病(COPD)的藥品做比對說明,如表二所示。
表二: 吸入溶液Lonhala Magnair跟Yupelri比較說明
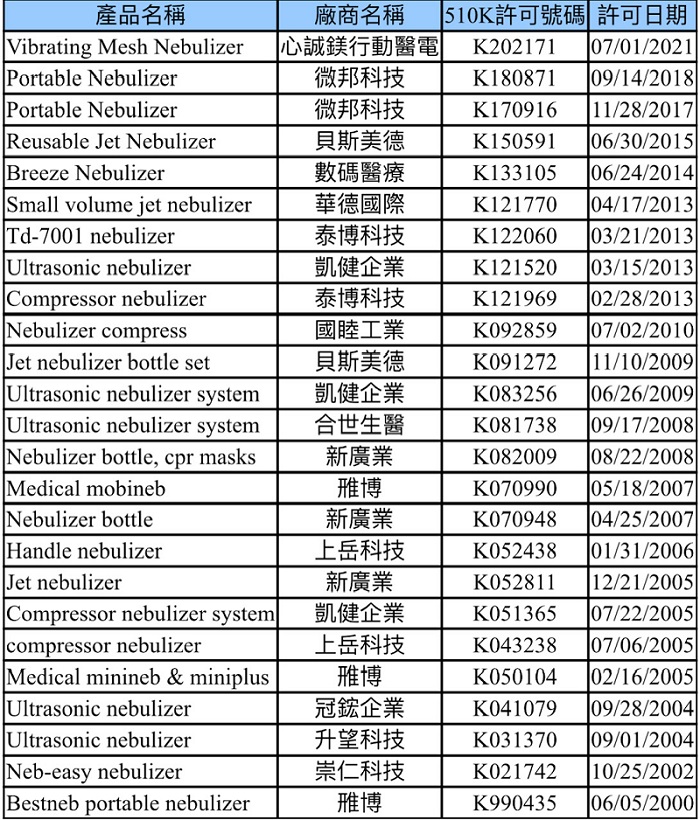
Lonhala與Yupelri的長效抗膽鹼製劑及適應症非常相似,所以兩者互為競爭者,有分析報告指出Yupelri吸入溶液產品的勝出的原因(9)如下:
- Lonhala只能使用PARI Magnair專用霧化器使用,較不方便。
- Lonhals吸入溶液通過聯邦醫療保險D部分報銷(與其他吸入藥物類似,如乾粉吸入器),使得保險報銷和納入處方籤更具挑戰,原因或與使用專用霧化器有關。相比之下,Yupelri可用於任何符合標準的噴射式霧化器,於醫院使用時可簡單地插入壓縮空氣系統。所以Yupelri較易獲得的聯邦醫療保險B部分支付。
- Lonhals每天使用兩次,而Yupelri每天只使用一次。
- Lonhals沒有公布與同為長效抗膽鹼製劑的噻托溴銨(Spiriva)藥物的比較,噻托溴銨是COPD病人標準治療藥物。而Yupelri官方公布臨床效果,對COPD病人惡化率降低了17%,且對第一秒吐氣容積(FEV1)單藥治療也勝過其他長效抗膽鹼製劑。
- 從理論上講,Lonhala搭配PARI Magnair專用霧化器具有優勢,因爲它有便携性,Yupelri使用的噴射式霧化器較笨重,另外Lonhala吸入的時間平均要2到3分鐘,Yupelri平均要8分鐘,但PARI Magnair專用霧化器清潔工作非常複雜,因此,用Lonhala進行吸入治療所消耗的總時間可能會比Yupelri多。
- 使用吸入藥物具複雜性,霧化治療的使用者通常是老年患者,需要重新學習使用PARI Magnair霧化器,因此可能會帶來困擾。在這種情況下,為患者提供一個易於使用且熟悉的霧化器將成為一個巨大的優勢。根據Yupelri的市場分析報告,美國約有9%的COPD病患者選擇一般霧化器進行治療,對於使用Yupelri的患者來說,不需要重新學習使用新的霧化器。
台灣針對霧化器產品發展現況
台灣霧化器廠商的新產品開發多以篩孔霧化器(Mesh nebulizer)為主,宣稱效果比噴射霧化器好,粒徑較小、給藥效率較高、較少藥品殘留等。效果雖然較好,但可能導致吸入藥量較高,有用藥過量的風險。這也是吸入溶液仿單上注意事項所提及當使用非建議的霧化器產品時,不能確保用藥的安全性及有效性。建議廠商開發一般使用的霧化器時,還是要以仿單上建議使用的霧化器,與其進行比對,證明自己的霧化器與仿單建議的霧化器具有實質相等性。
針對一般使用霧化器未來發展建議,根據美國FDA 510K資料庫查詢,市場相對飽和。醫療品牌大廠如歐姆龍(Omron)及飛利浦(Philips)均有多個霧化器產品取得美國510K許可,由於具品牌及價格成本優勢,已在美國市場佔有一席之地。
另如表一所示,台灣廠商最新一筆許可為「心誠鎂行動醫電」於2021年7月獲得許可,其次為「微邦科技」於2018年9月獲得許可,兩者相差約3年,這段時間也有幾家中國大陸廠商(深圳家瑞康、深圳來福士等)取得許可,如果台灣廠商產品不具特色及品質優勢,只能迫使降低價格吸引客戶。
針對藥物專屬霧化器未來發展建議,台灣也有廠商開發此類產品,例如霧化器新創廠商「利優生醫科技」(10),其霧化器平台AirHyper Platform具有兩項創新技術:AFDT (Adaptive Frequency Delivery Technology)利用自動優化的驅動頻率,可以驅動不同的液體來轉化成氣溶膠,縮短治療時間;DSMT (Digital Synchronized Monitor Technology)可記錄生理數據,根據病人的呼吸模式來驅動霧化器霧化給藥,可提高藥物遞送的效率。
另一家廠商「心誠鎂行動醫電」(11),有兩項產品Pulmogine及AdheResp,Pulmogine已有臨床一期的吸入生物藥合作案,用於治療非囊腫性纖維化支氣管擴張症;另與美國AeroRx Therapeutic合作開發全球第一款霧化吸入劑型的LABA/LAMA複方藥物,AeroRx公司將負責複方藥物劑型的開發、臨床試驗和商品化,心誠鎂負責AdheResp呼吸偵測式霧化器平台的客製化,此產品開發將依循505(b)2法規途徑,預計於2023年搭配心誠鎂的醫用霧化器進行人體PK/PD試驗。
國立清華大學生醫工程與環境科學系陳之碩副教授的智慧醫療霧化器(12)也獲得國科會2023年第 1 梯次科研創業計畫補助(13),該霧化器有幾項特點,如藉由改變驅動訊號之頻率模態方式,使霧化器產出小粒徑(extra-fine particle, 1-3微米)藥物;利用呼吸氣音觸發給藥搭配肺功能預判法,大幅提升使用者吸入藥物比率;氣音觸發僅在吸氣期間提供霧化藥物吸入,吐氣期間停止給霧,將大幅降低吐氣時患者病菌氣溶膠經由霧化顆粒帶出,能減少因吸入治療傳遞呼吸道疾病的臨床人員風險。
發展霧化器產品的挑戰與策略
對於想要進入吸入溶液霧化器複合式產品新市場的台灣廠商,其面臨的挑戰和困難如下:
- 技術要求:開發複合式產品需要同時具備藥學知識和霧化器技術,對於新的廠商可能需要進行大量的研發工作和技術投入。
- 藥廠合作:為了開發吸入溶液複合式產品,新的霧化器廠商需要與藥廠進行合作,確保其霧化器與特定藥品的配合性和相容性。藥廠可能會對新合作夥伴的技術和製造能力提出嚴格要求,以符合藥品申請的規範。
- 專利保護:複合式產品新藥或學名藥的開發可能涉及到專利保護的問題,特別是當原研藥廠已經與其他霧化器廠商簽訂專利合約時。新的霧化器廠商須仔細評估專利情況,避免侵權風險。
- 相關法規:新的霧化器廠商需要遵守相關的醫療器械法規和藥品規定,確保產品符合相應的安全和品質標準。這可能需要進行大量的法規審核和申請工作。
- 市場競爭:吸入溶液複合式產品市場競爭激烈,已經有一些著名的霧化器廠商與藥廠合作並建立了良好的市場地位。新的霧化器廠商需要在競爭激烈的市場中找到自己的定位和優勢,以吸引藥廠合作和贏得市場份額。
總而言之,開發吸入溶液複合式產品需要克服技術要求、藥廠合作、專利保護、相關法規和市場競爭等困難,霧化器廠商也需要投入足夠的資源和努力,才能成功推出產品上市,取得商機。
參考資料:
- A Guide to Aerosol Delivery Devices for Respiratory Therapists — 5th Edition
- Regulatory Perspectives for Device Development for Inhalation Combination Products
- US FDA 510(k) Premarket Notification
- Lonhala Magnair prescribing information.
- Yupelri prescribing information
- Sumitomo Pharma Integrated Report 2020.
- Theravance Biopharma May 2023 Investor Presentation.
- Lonhala Magnair product official website.
- Theravance: Why Yupelri Can Become A Blockbuster.
- 利優生醫科技股份有限公司AirHyper Platform
- 心誠鎂行動醫電股份有限公司產品
- 陳之碩教授團隊--海王星智慧醫療霧化器
- 國科會112 年第 1 梯次科研創業計畫補助名單 (萌芽案)